記者陳書璿/綜合報導
食藥署昨(3)日召開高端疫苗保護效益評估專家會議,與會專家14人一致決議認同高端疫苗符合保護效益,代表高端EUA保住了。卻引起衛福部國健署前署長、公衛專家邱淑媞痛批,「此舉是政府自證違法!」她說,捨棄2萬人以上規模的臨床試驗,而讓100萬國人當白老鼠,加上為了選舉提前審過保護力數據,怒斥「真的當全民是盤仔?」
邱淑媞在個人臉書指出,各國疫苗不僅須有第三期試驗的保護力數據才敢通過,美國甚至要等保護力報告通過最好的期刊審查、登出後才敢審查其EUA。一般第三期臨床試驗規模要達2萬人以上,不但表示有大型研究提供「保護力」數據,且有機會看到較罕見副作用以驗證其安全性,同時,也證明大量製造的疫苗品管數據穩定而良好。
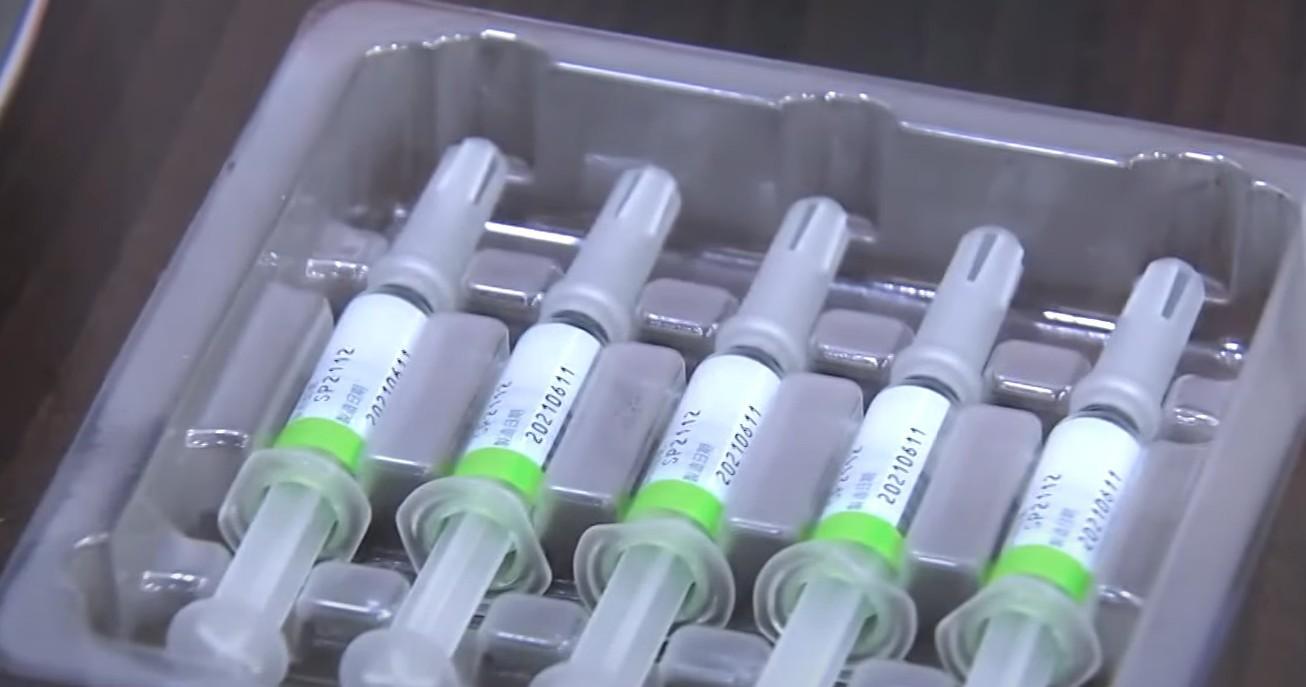
圖/翻攝自中天電視
邱淑媞說,更重要的是,第三期試驗的設計,必須透過「隨機分派」的對照組,以確保與實驗組的可比性,除了疫苗外其他條件並無差異,這樣的數據才乾淨、值得採信,是最高級的科學數據,這樣的研究設計提供的正確性無可取代。
「政府與高端,偏偏捨國際規範的正道不走。你不做隨機分派,那麼,100萬個國人當白老鼠所產生的數據,其科學等級,就是比2萬個人在正規的臨床試驗當白老鼠所能產生的數據等級矮一截。」邱淑媞氣憤地說。不僅科學上不合格且更嚴重違反人權,「哪有2萬個人的試驗不做,硬是讓100萬人當白老鼠的道理?可預期高端這個報告,上不了好期刊,沒有好期刊敢接受、刊登這樣的報告。」
至於高端在昨日被審查通過具有保護效益,邱淑媞反駁說,照國際規範去年7/18審查前,就應有保護力數據,「結果沒有,就『有條件』通過了,這本身已經是一個無效的通過。」有條件本身就宣告它還不具備通過條件。她怒斥一年內補報告是自欺欺人的作法,「更好笑的是,一年的時間又已經超過了。如果可以一延再延,那何必訂一年? 11/3過,不就是又自證違法一次?」
邱淑媞難以理解,本來要等選舉完才要審議,結果為了選舉提前審,「100萬人打進去,已經吐不出來了!」認為台灣的EUA已經在國際顏面掃地,「不撤銷,只不過是可以繼續買、繼續製造問題而已。真的當全民是盤仔?」